FDA 최초 승인 CRISPR 2.0(2세대 크리스퍼가위)
통합과학과 생명과학 개념으로 이해한 유전자 편집 치료제

메디컬저널
메디컬 현업 전문가팀
통합과학의 유전 질환, 생명과학1의 유전자 이상에 의한 유전병, 생명과학2의 생명공학기술과 유전자 가위 개념을 바탕으로, 최초의 FDA 승인 CRISPR 유전자 치료제인 Casgevy의 작용 원리를 살펴보았습니다. 특히 낫모양 적혈구 빈혈증의 원인이 되는 유전자 이상과 헤모글로빈 변화, CRISPR/Cas9의 유전자 편집 방식, BCL11A 조절을 통한 태아 헤모글로빈 증가 전략을 정리하고, 이를 통해 유전자 치료제가 기존 치료와 어떻게 다른지 이해하고자 하였습니다.
✔️ 안녕하세요, 의약계열 학종을 위한 가장 완벽한 콘텐츠 메디컬저널입니다. 메디컬저널은 네이처, 사이언스, 셀 등 저명한 유수의 학술지들을 비롯해 각종 논문과 전문서적의 어려운 학문적 내용들을 고등학생들이 직접 이해하고 활용할 수 있도록 풀어낸 학생 중심의 자료를 제작합니다.
2023년 12월 8일, 최초의 FDA 승인 CRISPR 유전자 치료제 탄생
FDA Approves First Gene Therapies to Treat Patients with Sickle Cell Disease
The FDA approved the first cell-based gene therapies, Casgevy and Lyfgenia, for the treatment of sickle cell disease in patients 12 years and older.
✔️ 지난 2023년 12월 8일 CRISPR 유전자 치료제가 최초 FDA 승인을 받았습니다. CRISPR/Cas 시스템을 인간의 유전자 편집의 도구로 활용할 수 있을 것이라는 2012년의 아이디어는 2020년 노벨 화학상 수상으로 이어졌고, 그로부터 얼마 지나지 않은 2023년 이를 활용한 최초의 의약품이 FDA 승인을 받게 된 것입니다.
품목허가 까지의 전체 신약 연구개발 기간이 평균적으로 10년 이상이 소요된다는 점에서 CRISPR/Cas 유전자 편집 기술은 매우 혁신적인 것임에도 매우 빠르게 품목허가까지 도달한 것이라 할 수 있으며 이는 그만큼 해당 기술에 대한 투자와 연구가 집중되어 왔음을 의미하는 것이라 할 수 있습니다.
⭐️ 이번 탐구에서는 통합과학, 생명과학1, 생명과학2 과목과 연계하여 CRISPR/Cas 유전자 치료제에 대해 자세히 살펴보도록 하겠습니다. 특히 최근 FDA 승인을 받은 두 품목 중 Vertex Pharmaceutical Inc의 Casgevy에 대해 자세히 살펴보도록 하겠습니다.
✔️ 의약 계열(의학 혹은 약학)에서의 질병과 그 치료에 대한 연구의 궁극적 목적은 전 인류의 생명을 존중하고 건강과 복지 그리고 행복을 증진시키기 위한 것이라 할 수 있다. 통합과학과 생명과학1 그리고 생명과학2 교과목에서 소개되는 낫 모양 적혈구 빈혈증의 경우 1900년대초 처음 발견되고 1957년 그 원인이 밝혀진 질병임에도 아직까지 근본적인 원인을 해결하는 뚜렷한 치료제가 없는 unmet needs에 해당한다. 이러한 인류 건강 문제에 관심을 가지고 탐구하며 해결책을 고민하고 연구하는 것은 의약학계에서 우선시 되어야 할 과제 중 하나라 생각하며 그러한 인식에서 CRISPR/Cas9 유전자 치료제가 낫 모양 적혈구 빈혈증을 적응증으로 FDA 최초 승인을 받았다는 기사를 보고 이에 대해 자세히 탐구해보고 싶은 생각을 가지게 되었다.
CRISPR 유전자 치료제의 현재
낫 모양 적혈구 빈혈증(Sickle Cell Disease, SCD)
# Unmet needs와 Orphan drug
“Sickle cell disease is a rare, debilitating and life-threatening blood disorder with significant unmet need, and we are excited to advance the field especially for individuals whose lives have been severely disrupted by the disease by approving two cell-based gene therapies today. Gene therapy holds the promise of delivering more targeted and effective treatments, especially for individuals with rare diseases where the current treatment options are limited.”
Nicole Verdun, M.D., director of the Office of Therapeutic Products within the FDA’s Center for Biologics Evaluation and Research.
✔️ 의료계에서 Unmet needs(혹은 Unmet medical needs)라 함은 어떤 질환의 진단이나 치료가 기존의 방식과 기술로는 부족한 미충족 의료 수요를 뜻하는 것으로, 즉 아직까지 유효한 치료법이 개발되지 않은 질병들에 해당합니다. 이러한 Unmet needs는 주로 희귀 질환(rare disease)에서 발생합니다. 생
명을 위협하거나 일상생활에 큰 지장을 주는 질병인 탓에 유효한 치료제에 대한 환자들의 강한 니즈가 존재함에도 10만명 이하의 낮은 유병률로 인해 연구개발이 진행되지 않은 경우가 많으며 기업에서도 수익성이 보장되지 않아 신약 연구개발을 꺼리는 탓에 희귀 질환 환자들의 니즈는 충족되지 못하게 됩니다.
세계보건기구 WHO에 따르면, 희귀질환은 7000가지가 보고되었으며, 환자 수는 3억 5000만명에 달한다고 합니다. 현재 약 1100개의 희귀의약품이 FDA 승인을 받았으나 발견된 희귀질환 중 약 90% 이상은 여전히 치료제가 없는 상황입니다.
❗️이러한 희귀의약품을 FDA는 'Orhpan drug'라 부르며, 미 FDA는 이러한 희귀질환들에 대한 의약품 연구개발을 장려하기 위한 법률(The Orphan Drug Act)을 제정해 시행하고 있습니다. FDA 에 의해 희귀의약품으로 지정(Orphan Drug Designation, ODD)되려면 환자수가 10만명 이하인 희귀 질환이어야 하며 미충족 의료 수요가 높은 질병이어야 합니다. 희귀의약품으로 지정(ODD)되는 경우 ① 연구 개발 비용의 25%(임상 비용의 50%)가 세액 공제되며 ② 시판 후 7년간 시장 독점권을 부여 받는 등의 혜택을 받을 수 있습니다.
❗️ 또한 FDA는 심각한 질환(Serious disease) 혹은 희귀 질환(rare disease) 치료제의 연구개발이 신속하게 진행될 수 있도록 하는 '신속 심사 프로그램(FDA's Expedited Drug Approval Programs)을 운영하고 있습니다. 해당 프로그램은 ① Fast track, ② Breakthrough Theray, ③ Accelerated Approval, ④ Priority Review 네가지 제도로 운영됩니다.
① Fast track은 주로 Unmet needs를 대상으로 하는 의약품에 한하여 개발과정에서 FDA와 더 빈번한 소통이 이루어지며 그에 따라 연구개발 과정을 빠르게 진행할 수 있는 이점이 있습니다.
② Breakthorugh Therapy(혁신 신약)는 생명을 위협하는 심각한 질환에 대해 임상시험 초기 결과가 기존의 치료법보다 우월성이 있다고 여겨지는 의약품에 한하여 FDA가 더 intensive한 가이드를 제공하여 연구개발이 빠르게 진행될 수 있도록 하는 제도이며,
③ Accelerated Approval은 심각한 질병에 대한 Unmet needs를 대상으로 하는 의약품에 한해 임상시험이 완전히 끝나지 않은 상황에서도 대리 지표를 통해 그 결과를 예측할 수 있는 경우 임상 2상 이후 빠르게 의약품을 승인해주는 제도입니다. (※ 단, 지난 코로나19 백신의 긴급승인(EUA)와는 다른 것입니다. 긴급승인은 공중보건 비상사태에서 질병에 대응하기 위한 것입니다)
④ Priority Review는 기존의 치료법에 비해 안전성과 유효성 측면에서 유의미한 발전이 있는 의약품에 한하여 품목허가 승인신청(NDA, New drug application) 검토의 과정을 기존의 10개월에서 6개월로 단축해 주는 것을 의미합니다.

⭐️ 이제 우리는 CRISPR/Cas 유전자 편집 기술을 이용한 치료제가 이렇게나 빨리 탄생한 이유 중 하나를 설명할 수 있습니다. 이번에 승인을 받은 두 치료제는 모두 낫모양 적혈구 빈혈증(SCD)를 적응증(치료 대상 질환)으로 하고 있습니다.
낫모양 적혈구 빈혈증은 1957년 그 원인이 밝혀졌지만, 여전히 그 본질적 원인(유전자 이상)을 해결하는 마땅한 치료제가 없는 희귀 질환에 해당하며 주로 선진국이 아닌 아프리카에서 발병한다는 것 또한 unmet needs가 존재하는 하나의 이유가 됩니다.
→ 이러한 이유로 이번 승인 의약품 2가지는 모두 희귀 의약품으로 지정(ODD) 되어 다양한 혜택을 받는 것과 동시에 연구개발 과정에서 Fast track을 적용받아 FDA와의 소통과 함께 빠르게 연구개발이 진행되었으며 또한 Priority Review에 의해 품목허가 승인 검토가 기존의 10개월이 아닌 6개월만에 이루어져 2023년 12월에 품목허가가 이루어질 수 있었습니다.
# 원인과 증상
✔️ 낫 모양 적혈구 빈혈증에 대해서는 고1~고3(통합과학, 생명과학1,2)에 모두 소개되고 있습니다. 그 이유는 낫 모양 적혈구 빈혈증이 유전자 이상에 의한 대표적 유전병이기 때문일것입니다.
❗️낫 모양 적혈구 빈혈증은 유전자 돌연변이로 인해 DNA의 염기 T(타이민)이 A(아데닌)으로 변하게 되고, 그 결과 코돈이 변하여 극성 아미노산 글루탐산이 아닌 비극성 아미노산 발린으로 번역이 이루어지게 됩니다. 이러한 아미노산의 변화는 헤모글로빈을 구성하는 베타 사슬(헤모글로빈은 2개의 알파사슬과 2개의 베타사슬로 구성됩니다)의 변화를 일으키고, 이는 헤모글로빈의 구조 변화를 야기하며, 결국 헤모글로빈으로 구성되는 적혈구의 모양이 낫 모양으로 변화하게 됩니다.
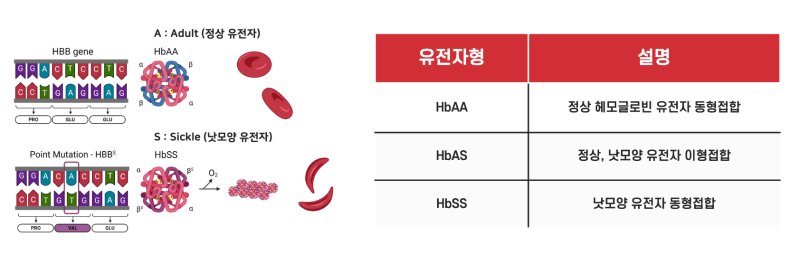
⇢ 헤모글로빈의 유형을 유전자형으로 나타낼 수 있습니다 이때 A는 정상 성인 헤모글로빈 유전자를 의미하며, S는 낫모양 유전자를 가지는 것을 의미합니다. 따라서 HbAA라 함은 정상 성인 헤모글로빈 유전자를 동형접합으로 가진 헤모글로빈 유형을 의미하며, HbAS는 정상과 낫모양의 이형접합, HbSS는 낫모양 유전자의 동형접합인 헤모글로빈 유형을 의미합니다.
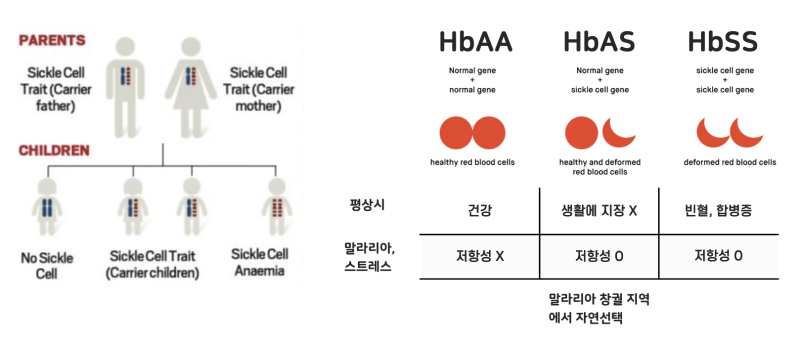
⇢ 이처럼 낫 모양 적혈구 빈혈증은 유전자에 의해 결정되는 형질이며, 부모에서 자식으로 유전되는 유전병에 해당합니다. HbSS(낫 모양 동형접합)는 낫 모양 적혈구 빈혈증 형질에 해당하며, 그 증상은 적혈구가 낫모양으로 변함에 따라 산소 운반능력이 떨어져 빈혈으로 극심한 통증을 유발하게 되고 또한 낫모양으로 변한 적혈구가 혈관을 막는 Vaso-occlusive events(VOEs)가 발생하여 전신의 합병증을 유발할 수 있습니다.
이러한 VOEs는 지속적으로 재발할 수 있다는 점에서 낫 모양 적혈구 빈혈증은 생명에 위협을 끼치는 심각한 희귀 질병이며 최근 승인된 CRISPR 유전자 치료제는 이러한 형질을 대상으로 합니다.
※ 이때 HbAS(이형접합)은 Sickle Cell Trait이라 불리는데, 이들은 정상 성인 헤모글로빈 유전자를 1개 가지므로 평상시에는 헤모글로빈이 낫모양으로 변화하지 않고 따라서 산소 운반이 충분하여 생활에 지장이 없습니다. 그런데 말라리아(적혈구에서 증식)에 감염되거나 혹은 극도의 스트레스, 체력 고갈 등의 상황에서는 적혈구 모양이 낫모양으로 변화하여 빈혈을 유발하게 됩니다.
낫모양으로 변한 적혈구에서는 말라리아가 증식하지 못하므로 말라리아 저항성을 가지게 되며 이러한 이점으로 인해 해당 형질이 말라리아가 창궐하는 지역에서는 자연선택 되는데, 이는 결국 낫 모양 헤모글로빈 유전자 S가 사라지지 않고 존재하게 합니다. 평상시에 생활에 지장이 없으며 말라리아에 저항성을 가지는 HbAS 형질의 두 부모 사이에서 유전에 의해 낫 모양 적혈구 빈혈증의 자식이 태어날 수 있는데, 이러한 자연선택과 유전의 원리가 아프리카 특정 지역에서 낫 모양 적혈구 빈혈증(HbSS)이 주로 발생하는 이유가 됩니다.
# 치료 전략
앞서 설명한 것 처럼, 낫 모양 적혈구 빈혈증(SCD)는 현재까지 유효한 치료제가 없었던 희귀 질환에 해당하며, 그것이 이번 CRISPR 치료제가 희귀 의약품(Orphan drug)으로 지정된 이유가 됩니다. 기존의 치료제들의 대부분은 단지 낫 모양 적혈구 빈혈증으로 인해 나타나는 증상을 완화하거나(대증요법) 혹은 합병증을 관리하는 차원이었다면, CRISPR/Cas 치료제는 형질의 원인이 되는 유전자를 타겟으로 하여 질병의 원인을 고친다는 핵심적 차이가 있습니다.
❗️ 유전자 치료에 의해 낫 모양 적혈구 빈혈증을 치료하는 전략은 2가지로 분류해볼 수 있습니다.
① Gene correction
첫번째로 원인이 되는 유전자를 교정하는 방식입니다. 구체적으로는 염기 점 돌연변이에 의해 T로 변한 A를 다시 T로 바꾸는 것입니다. 이러한 방식은 매우 이상적이라 생각될 수 있지만, 기술적으로도, 또한 이론적으로도 매우 복잡하다는 한계를 지니고 있습니다. * 이론적으로 복잡하다는 것은, 예를들어 어떤 질환을 치료하기 위해 유전자를 교정하였을때, 변화된 유전자에 의해 또 다른 질병이 발생할 수 있다는 것을 의미합니다.
남들과 다른 세특, 어떻게 시작할지 막막하다면?
세특 탐구 특화 아카AI로 나만의 주제 추천받으세요.
